|
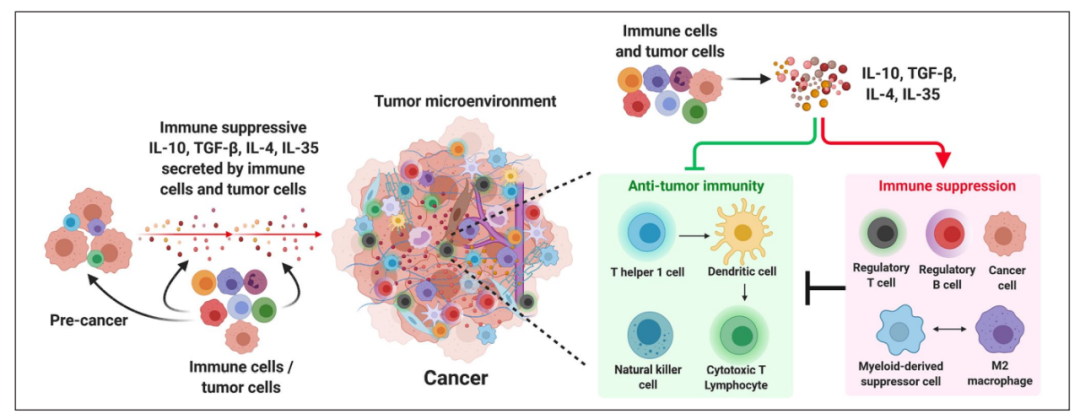
通过各种方式激活NK细胞,如双特异抗体,CAR-NK等是目前研究的一个方向戒烟激活癌细胞,本片文章我们主要介绍一下目前激活NK细胞的双特异抗体的开发现状。 NK细胞概述及抗肿瘤作用机制 NK细胞是先天性免疫系统的组成部分,为身体免疫系统的第一道防线。其在体内巡视,并被招募到肿瘤部位消灭肿瘤细胞。研究表明,在多种肿瘤微环境中如黑色素瘤、神经母细胞瘤、肝细胞癌、肾细胞癌、胃癌、乳腺癌、乳腺癌、腺癌肺癌、鳞状细胞肺癌,以及非小细胞肺癌等,NK的浸润与患者更好的总生存率有关。 根据NK细胞表面CD56抗原的表达水平,其可以分为两个亚群:1) NK细胞储存预先形成的细胞毒性效应蛋白(包括穿孔蛋白和颗粒酶B),表达高水平的CD16A(FcγRIIIa),并迅速介导强大的细胞溶解功能;2) NK细胞表达低水平的CD16A并在细胞因此的刺激下产生产生大量的IFN-γ和其它因子。 除了直接的抗肿瘤活性外,NK细胞还能产生细胞因子和趋化因子,可能激活多种免疫细胞如DCs和T细胞。如其通过产生CCL5、XCL1/2和,促进招募cDC1s(专门将肿瘤抗原交叉呈递给CD8+T细胞的DC亚群)TME。研究表面,NK细胞不仅在抗肿瘤CD8+T细胞的激活中起着关键作用,而且可能在促进T细胞效应和对肿瘤持久控制方面具有重要作用。
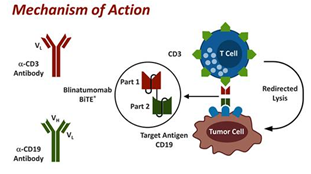
在临床中, NK细胞发挥抗肿瘤作用主要是通过IgG1型的抗体。 IgG1型抗体结合肿瘤表面的抗原后主要是通过Fc端诱导的ADCC,CDC或者ADCP等作用发挥抗肿瘤作用。而其中ADCC作用的发挥是通过Fc于FcγR结合,如NK细胞的表面发CD16A。 目前已经有30多款IgG1单克隆抗体获批上市用于肿瘤的治疗戒烟激活癌细胞,如, ,等。这些抗体在肿瘤的治疗中发挥了巨大作用,但是在部分肿瘤相关抗原表达较低,或者抗原表达下调的病人中,这些抗体无法发挥ADCC等作用,因此限制的抗体的治疗效果。 目前已经有多种方法用于增强部分治疗性抗体的ADCC效应,如通过Fc的点突变,增加Fc与FcγR结合的结合力,或者降低抗体的岩藻糖增加抗体Fc与FcγR 的结合力等。 NK细胞受体及其双抗开发现状 除了我们熟知的CD16A外, NK细胞还表达其它一些激活性受体,如NKG2D ,CD94/NKG2C 和自然杀伤受体(NKp30, NKp44,和 NKp46)等,下面我们详细介绍一下这些受体及其双抗的开发现状。 CD16A-NKCEs CD16A是免疫球蛋白超家族的一个成员,有两个胞外Ig样结构。它在NK细胞、肥大细胞、巨噬细胞和单核细胞上表达,并作为IgG抗体Fc片段的受体。抗原结合的IgG与CD16A相互作用,诱导其细胞内基于免疫受体酪氨酸的磷酸化。这种磷酸化引起的依赖激酶的信号级联传导并引起相关效应细胞发挥功能。CD16A多态性(V158F)改变了与IgG的结合亲和力,是造成个体间免疫差异的基础。研究表明CD16A的158V的异构体与Fc结合能力更强且与患者的临床结果呈正相关。 目前 已经有多个靶向CD16A的双特异抗体正在研究中, 如公司通过BiKE和TriKE平台构建的双特异抗体,其构建方式如下图所示,抗体主要由scFv组成,通过连接。TriKE是对BiKE双特异抗体平台的升级改造,引入了能够刺激NK细胞增值,存活的IL-15抗体,从而在一定程度上增强NK细胞对肿瘤细胞的杀伤能力。目前该平台GTB-3550(CD16a-IL-15/CD33)已经进入临床 其中AFM13是进展最快也是值得期待的一款双抗,目前处于临床Ⅱ期,用于治疗外周T细胞淋巴瘤、转化型蕈样变性和霍奇金淋巴瘤。在一项针对复发或难治性霍奇金淋巴瘤患者的I期试验中,AFM13具有良好的耐受性。AFM13在输液后可诱导外周血中的NK细胞激活,并具有一定的抗肿瘤活性。在≥1.5mg/kg的患者中,总反应率为23%,疾病控制率为77%。在一项治疗复发或难治性霍奇金淋巴瘤的Ib临床研究中,AFM13与的联合治疗产生了88%的客观反应率,总反应率为83%。
NKG2D-NKCEs NKG2D(KLRK1)是一种凝集素型家族的激活受体。它表达在NK细胞、NKT细胞、γδ T细胞亚群和CD8+T细胞亚群上。NKG2D是一个由两个二硫键连接的同源二聚体跨膜蛋白,其细胞内结构域很短,没有信号传导功能。在人类中,NKG2D受体不含有ITAMs,也不与含有ITAMs的适配体,而只与适应体蛋白DAP10结合。(图2)。DAP10的信号传导与ITAM所引起的信号传导截然不同,因为它诱导招募和激活了磷脂酰肌醇-3激酶(PI3K)。NKG2D与一些MHCI-结合,包括MICA、MICB和ULBP家族的六个成员。NKG2D配体通常以较低的丰度存在于正常细胞的表面,但在感染和肿瘤发生时可以被诱导。NKG2D在NK细胞上被细胞结合的配体激活,诱发细胞毒性。 NKG2D触发细胞因子分泌的能力仍不清楚,因为mAb介导的NKG2D的交联无法诱导细胞因子的分泌,但与此相反,用可溶性重组NKG2D配体(MICA, ULBP-1, or ULBP-2)刺激可诱导IFN-γ、GM-CSF和MIP-1β的表达。有学者认为,NKG2D与高亲和力的配体结合交联时才能被激活释放相关细胞因子。NKG2D生物学中的一个重要观点是,它的下调是由长期与其同源的细胞表面配体接触所引起的,而这种下调可以诱导NK细胞脱敏。NKG2D配体的可溶性形式也可以从肿瘤细胞表面脱落后或通过外泌体产生,但其生物学功能仍不清楚。 有研究者构建了同时靶向CS1和NKG2D的双特异抗体,并且在体内外实验中都展现了良好的效果。
NKp30-NKCEs NKp30(NCR3,CD337)是一个属于免疫球蛋白超家族的I型跨膜激活受体。它表达在幼稚和活化的NK细胞、ILC2、CD8+T细胞的一个亚群和γδ T细胞。NKp30通过与与含有ITAM功能的CD3ζ和FcR分子的结合来介导信号传导。NKp30的激活导致了细胞毒性的产生和NK细胞分泌细胞因子。表面分子B7-H6和核因子HLA-B相关转录物3(BAT3,又名BAG6),从肿瘤细胞中释放出来,并且可以结合并激活NKp30。 B7-H6似乎对肿瘤细胞具有特异性,因为它在正常细胞上几乎检测不到,但在在多种肿瘤细胞系上高表达。与NKG2D配体一样,可溶性B7-H6可以在各种癌症患者中检测到,并且可溶性B7-H6的存在与NK细胞NKp30的下调有关。 CTX-8573是靶向NKp30和BCMA的双特异性抗体,其结构如下图所示,抗体的C末端连接抗NKp的Fab,并且利用相同的轻链解决错配问题,为了进一步增强NK细胞的作用,其Fc端采用了去岩藻糖处理。CTX-8573已被证明在体外和体内具有抗肿瘤的功效。 NKp46-NKCEs 目前NKp46双特异抗体的开发都处于临床前研究,国际上主要有两个公司在开发相应的抗体 (CYT-303和)和 (和IPH21)。 总结 与激活T细胞的双特异抗体及CAR-NK疗法相比,靶向激活NK细胞的双特异抗体开发才刚刚起步。而且在国内,只有少数几个公司有相关研究。 参考文献: , , and Eric 。 cell in :Next of - . Eur. J. . 2021. 51: 1934 –1942 请注明:姓名+研究方向! 版 权 声 明 (责任编辑:admin) |